주요한 차이점 : 확산은 분자가 대량 이동을 필요로하지 않고 한 장소에서 다른 장소로 이동하고 이동하는 과정입니다. 유출은 분자가 핀홀을 통해 고농도에서 저농도로 이동하는 과정입니다.
용어 확산 및 삼출은 화학, 물리학 및 생물학과 같은 많은 과학에서 일반적으로 사용됩니다. 화학에서이 두 용어는 가스의 두 가지 특성입니다. 이 두 가지는 가스의 기초와 특성을 배우는 많은 사람들에게 혼란 스럽습니다. 확산과 유출은 서로 다른 두 가지를 의미하며 서로 교환 할 수 없도록 사용해야합니다. 확산은 가스가 서로 섞일 수있는 능력을 말하며, 유출은 가스가 작은 핀홀을 통과하는 능력을 나타냅니다. 확산은 또한 사회학, 경제학 및 금융에서 사람, 아이디어 및 가치의 보급을 나타 내기 위해 사용됩니다.
확산은 분자가 대량 이동을 요구하지 않고 한 장소에서 다른 장소로 이동하고 이동하는 과정입니다. 확산은 운동 에너지만을 사용하여 분자의 이동 또는 혼합을 초래합니다. '확산'이란 단어는 "확산"을 의미하는 "diffundere"라틴어 단어에서 파생됩니다. 확산에서 분자는 일정한 운동 상태에 있고, 운동 에너지 또는 열 에너지에 의해 추진 될 때 다른 분자와 섞여서 분리 할 수없는 혼합물을 생성하는 경향이 있습니다. 실용적인 접근법을 취해 보겠습니다. 하나의 컨테이너는 단색 파티션을 사용하여 A & B 섹션으로 나누어 져 있습니다. 제 1 섹션은 물로 채워지는 한편, 제 2 섹션은 적색 염료로 채워진다. 이제 칸막이가 들어 올 때 염료와 물이 전체 용기를 채 웁니다. 그러면 염료가 물을 붉게합니다. 이것은 확산입니다.
확산으로 인해 분자가 고농도 영역에서 저농도 영역으로 이동하여 모든 분자가 혼합됩니다. 모든 분자가 고르게 퍼지면 확산이 멈 춥니 다. 확산은 물에 국한되지 않고 분자가 다른 분자와 더 많은 에너지와 혼합 능력을 가진 기체 상태에서 가장 잘 작용합니다. 확산에는 두 가지 접근법이 있습니다 : 현상 학적 및 원자 적. 현상 학적 접근법에 따르면, 분자는 고농도 영역에서 저농도 영역으로 이동합니다. 원자 론적 접근법에서 확산은 확산 입자가 무작위로 걷는 현상으로 인해 발생하는 것으로 간주됩니다. 확산은 열에너지에 의해 추진되어 함께 혼합됩니다. 확산은 신체가 필요로하는 미네랄, 영양소 및 에너지를 생성하는 데 중요한 역할을합니다.

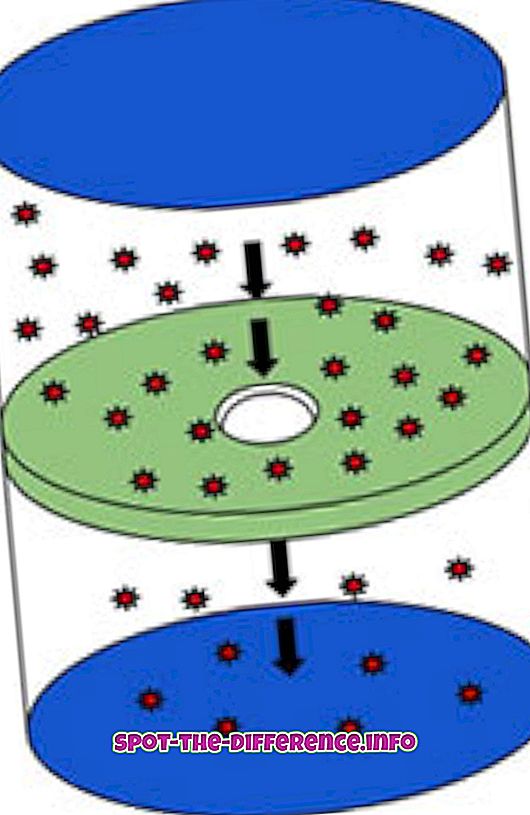
유출은 분자가 핀홀을 통해 고농도에서 저농도로 이동하는 과정입니다. 이 과정은 가스가 분자 사이의 충돌없이 작은 구멍을 통해 이동하는 능력을 설명합니다. 이것은 구멍의 직경이 분자의 평균 자유 경로보다 상당히 작은 경우 발생합니다. 평균 자유 경로는 연속적인 충돌 사이에서 움직이는 입자가 이동 한 평균 거리입니다. 이것을 실용적으로 보여주는 한 가지 예는 용기에 병을 채우고 병에 작은 구멍을 뚫는 것입니다. 구멍 밖으로 흘러 나오는 연기는 삼출액으로 간주됩니다.
유출을 측정하기위한 공식을 만든 스코틀랜드의 화학자 토마스 그레이엄 (Thomas Graham)에 따르면, 가스가 얼마나 빨리 이동하고 측정 할 수 있는지를 결정하는 그레이엄 법칙이 만들어졌습니다. 그레이엄의 법칙에 따르면, 가스가 빠져 나가는 속도는 분자량에 달려 있습니다. 분자량이 낮은 가스는 분자량이 높은 가스보다 빨리 방출됩니다. 누출은 얼마나 많은 분자가 1 초 안에 구멍을 통과 하는지를 측정함으로써 계산됩니다. 유사하게, 열역학에서 가스의 유출 속도는 입자의 질량의 제곱근에 반비례합니다.