주요 차이점 : 원자는 모든 문제가 만들어지는 기본 단위입니다. 서로 다른 원소의 원자들이 모여 분자를 만든다. 이것은 화학 반응을 통해 발생합니다. 분자는 존재할 수있는 화학 물질의 최소량입니다. 본질적으로 화합물은 분자의 한 유형입니다. 분자는 동일한 원소의 2 개 이상의 원자 또는 다른 원소의 2 개 이상의 원자로 구성 될 수 있습니다. 그러나 화합물은 다른 분자의 원자로 구성된 분자입니다.
원소는 하나 또는 하나의 유형의 원자를 가지며 원자 번호로 구별되는 순수한 화학 물질입니다. 원자 번호는 원소의 핵에 존재하는 양성자의 수에서 파생됩니다. 금속, 준 금속 및 비금속으로 구분 된 총 118 개의 원소가 확인되었습니다. 각 요소에는 고유 한 속성 집합이 있습니다. 대부분의 요소는 지구에서 사용 가능하지만 일부는 원자력 반응을 통해 인위적으로 개발되었습니다. 요소가 이미 원시 형식이므로 더 이상 분해 할 수 없습니다. 모든 요소는 원자 번호로 나열된 주기율표에서 찾을 수 있습니다.
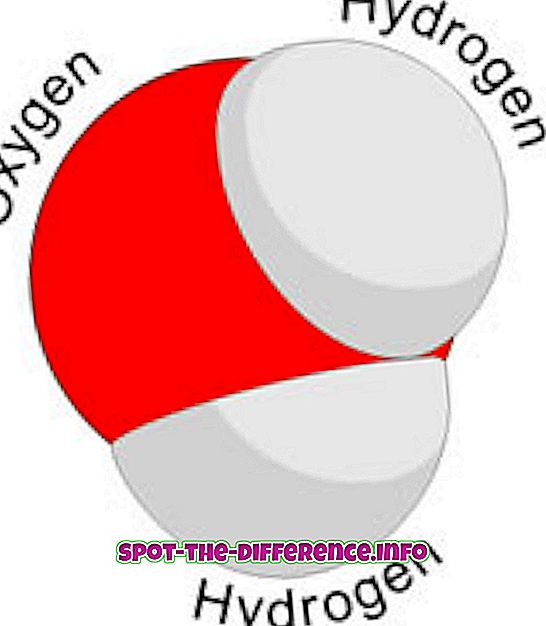
서로 다른 원소의 원자들이 모여 분자를 만든다. 이것은 화학 반응을 통해 발생합니다. 예를 들어 두 개의 수소 원자와 하나의 산소 원자가 결합하여 물 분자를 만듭니다.
분자는 존재할 수있는 화학 물질의 최소량입니다. 그러한 물의 최소량은 물 또는 H2O 분자 일 수 있습니다. 그것은 서로 다른 원자들로 이루어져 있습니다. 그러므로 그것은 다시 다른 원자들로 분리 될 수있다.
분자는 그것이 만들어내는 원소와 매우 다른 성질을 가질 수 있습니다. 예를 들어, 물은 수소 원자와 수소 원자 두 개로 이루어져 있어도 산소 나 수소와 매우 다르게 행동합니다.
또한 원자는 무언가에 결합하지 않고 자연에서 독립적으로 존재할 수 없습니다. 우리는 단지 하나의 산소 원자 또는 하나의 탄소 원자를 찾지 않을 것입니다. 그것은 항상 O2 (산소) 또는 CO2 (이산화탄소)와 같은 것으로 결합되어 있습니다. 분자에 결합 될 때 분자는 자연에서 독립적으로 존재할 수 있습니다. 따라서 우리는 항상 산소 분자, 이산화탄소 분자, 물 분자 (H2O) 등을 발견 할 수 있습니다.

분자들은 항상 함께 그룹화되는 경향이 있으며, 그들의 상태에 따라 형성됩니다. 기체 상태에서와 같이, 분자는 그냥 날아 다니는 경향이 있습니다. 액체 상태에서 분자는 느슨하게 그룹화되어 움직일 수 있습니다. 고체 상태에서, 분자들은 함께 단단히 묶여 진동 만 할 수 있습니다.
분자는 대개 분자식으로 표현됩니다. 예 : O2, H2O, CO2, C6H12O6 (설탕). 분자 공식은 원소의 이름이며 그 다음에 분자의 원소의 원자 수를 따른다.
본질적으로 화합물은 분자의 한 유형입니다. 분자는 동일한 원소의 2 개 이상의 원자 또는 다른 원소의 2 개 이상의 원자로 구성 될 수 있습니다. 그러나 화합물은 다른 원소의 원자들로 구성된 분자입니다. 따라서 모든 화합물은 분자라고 말할 수 있지만 모든 분자가 화합물은 아닙니다.
따라서 수소 (H2), 산소 (O2), 질소 (N2), 물 (H2O), 이산화탄소 (CO2) 및 메탄 (CH4)은 모두 분자입니다. 그러나 물 (H2O), 이산화탄소 (CO2) 및 메탄 (CH4)만이 화합물이며 다른 것들은 화합물이 아닙니다.