주요 차이점 : 몰 농도는 몰 농도라고도하며 용액 1 리터당 존재하는 물질의 몰수를 측정합니다. 양극성은 M으로 표시됩니다. Molality는 용매 1kg 당 존재하는 물질의 몰수를 측정합니다. Molality는 소문자 m으로 표시됩니다.
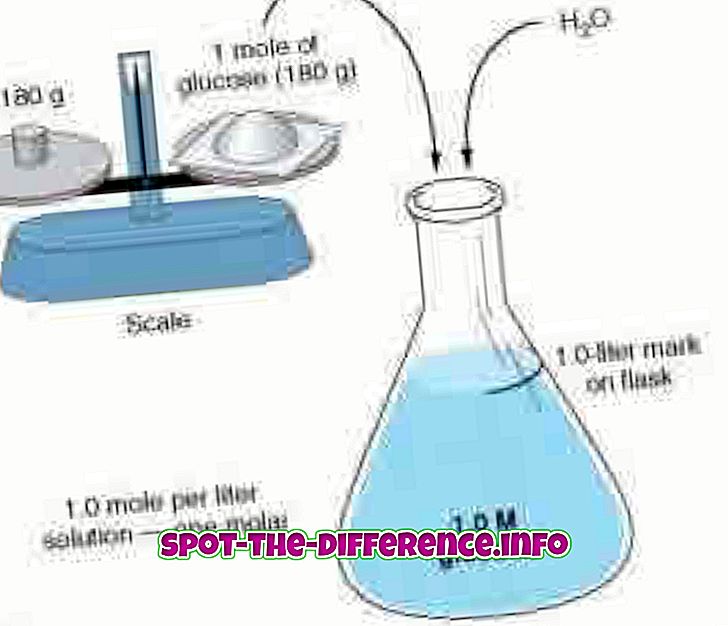
이 두 가지 개념은 현재 솔루션에 얼마나 많은 두더지가 있는지에 대한 계산을 기반으로합니다. 솔루션은 균질 혼합물로 정의 할 수 있습니다. 이는 두 개 이상의 구성 요소가 육안으로 구별 될 수없는 지점까지 섞여 있음을 의미합니다. 이 두 가지 개념은 용액에 존재하는 몰수를 결정할 때 몰수를 이해할 것을 요구합니다. 두더지 이론은 이탈리아 과학자 Amedeo Avogardo에 의해 발견되었습니다.
1811 년에, Avogardo는 주어진 온도와 압력에서 가스의 부피가 그 성질에 관계없이 원자 또는 분자의 수에 비례한다고 제안했다. 이 개념은 Avogardo 상수로 알려져 있습니다. 이것은 주어진 물질 1 몰당 구성 입자 (보통 원자 또는 분자)의 수로 정의됩니다. 평범한 용어로, 한 몰의 물질은 원소 속에 존재하는 원자와 분자의 수를 나타낸다. 예 : 산소는 원자량이 16이며, 이는 산소 1 몰당 질량을 나타냅니다. 따라서 1 몰의 산소는 16 그램의 질량을 갖습니다. Avogardo에 따르면, 1 몰의 산소는 1 몰의 수소와 같은 수의 원자를 가질 것입니다. 그러나 체중이 다를 수 있습니다.
양극성과 몰 성적은 두 가지 다른 접근법을 사용하여 농도를 측정합니다. 몰 농도 (몰 농도)는 용액 1 리터당 존재하는 물질의 몰수를 측정합니다. 양극성은 자본 M으로 표시됩니다. 따라서 1.0M 용액은 용액 1 리터당 1 몰의 용질을 함유하고 있다고 말합니다. 예 : 물과 설탕의 용액. 용액이 1.0M으로 측정되는 경우, 용액은 존재하는 용액 1 리터 당 1 몰의 설탕을 갖는다. 양극성은 물질의 양, 농도, 물질 농도 또는 단순히 농도로 알려져 있습니다. Molarity는 다음 공식을 사용하여 계산할 수 있습니다. M = mol (몰의 수) / L (용액의 부피).

몰 랄성은 용매 킬로그램 당 존재하는 물질의 몰수를 측정합니다. Molality는 소문자 m으로 표시됩니다. 따라서 1.0m 용액은 용매 1kg 당 1 몰의 용질을 함유하고 있다고 말합니다. 용매와 용질을 구별합시다. 용질은 다른 물질에 용해되는 물질입니다. 용제는 용질을 용해시키는 물질입니다. 따라서 물과 설탕을 함께 섞으면 설탕은 용질이 될 것이고 용제는 물이 될 것입니다. 혼합 된 설탕 물이 해결책이 될 것입니다. 이제 몰몬은 moles가 용매가 아닌 용액의 질량으로 나뉘는 것이 가장 중요합니다. molality는 다음 공식을 사용하여 계산할 수 있습니다. m = mol (몰의 수) / KG (용매의 질량 (kg)).
차이점은 무엇입니까? 음, 둘 다 온도를 다룰 때 사용됩니다. 용액의 온도가 변하면 몰리 력이 사용됩니다. 그러나 일정한 온도 몰 농도로 유지되는 용액이 사용됩니다. 이는 온도가 상승하거나 하강 할 때 용액의 부피가 변화하고 이것이 몰 농도에 직접적으로 영향을 미치기 때문입니다. 따라서 몰 농도는 농도를 계산하는 데 사용됩니다.