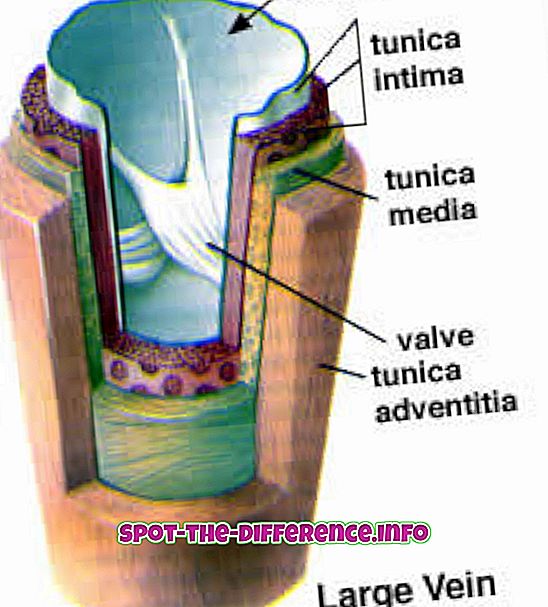
주요 차이점 : 화학 반응은 원소의 원자가 재 배열되어 새로운 물질을 형성하는 과정입니다. 핵 반응은 원자의 핵 구조가 에너지의 방출과 함께 변화되는 과정이다.
핵 반응과 화학 반응의 주된 차이점은 '어떻게 반응이 원자에서 일어나는가'에 기초하여 이해 될 수있다. 핵반응은 원자핵에서 일어난다. 원자의 전자는 화학 반응을 담당합니다.
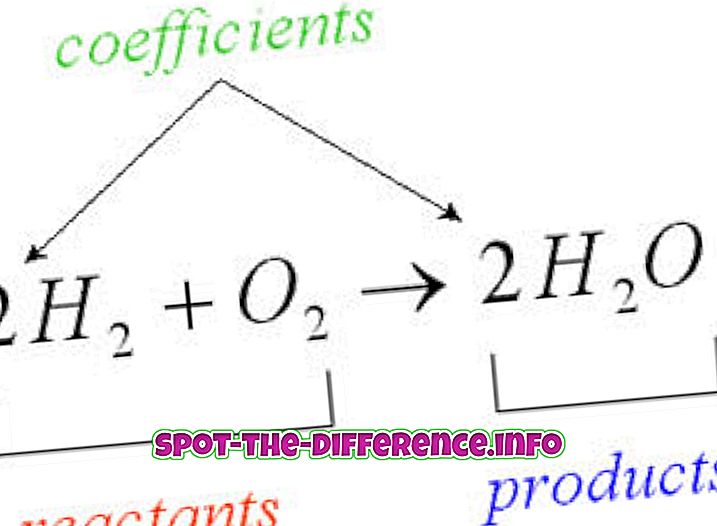
촉매, 온도, 용매 효과 등과 같은 방정식을 제어하는 다양한 요소가 있습니다. 열역학 연구를 통해 반응을 제어 할 수 있습니다. 반응 속도는 단순히 반응의 속도를 결정합니다. 이것은 반응이 얼마나 느리거나 빠름을 연구하는 매개 변수입니다. 예를 들어,
반응물 A와 B가 생성물 C와 D로 들어가는 다음의 반응을 고려하십시오.
a a + b B → c C + d D
반응 속도는 2 개의 반응물 또는 생성물 중 어느 하나의 관점에서 주어질 수있다.
Dt = 1 / c × d [C] / dt = 1 / d × d [D] / dt
여기서, a, b, c 및 d는 반응물 및 생성물의 계수이다. 반응물의 경우, 없어지 기 때문에 빼기 기호가 있습니다.
반응이 진행됨에 따라 그러나 제품이 증가함에 따라 긍정적 인 징후가 나타납니다.

핵 반응은 원자를 분해 할 때 핵의 분해를 포함한다. 그것은 양성자 또는 중성자의 손실로 새로운 요소를 형성합니다. 반응은 핵 내부에서 일어난다. 핵 반응에는 매우 높은 에너지 변화가 있습니다. 그것은 핵융합과 핵분열로 나눌 수있다. 융합에서 두 가지 유형의 핵이 결합되어 에너지를 방출합니다. 핵분열에서, 큰 불안정한 핵은 두 개의 더 작은 안정한 핵으로 분할되고 에너지가 방출된다.
화학 반응과 핵 반응의 비교 :
화학 반응 | 핵반응 | |
정의 | 요소가 다시 정렬되어 새로운 요소를 형성합니다. | 에너지의 방출에 따라 핵의 구조가 변화합니다. |
반응 | 전자는 반응을 담당한다. | 그것은 원자의 핵에서 일어난다. |
위치 | 그것은 핵 밖에서 발생합니다. | 그것은 핵 내부에서 일어난다. |
자연 | 전자의 손실, 이득 및 공유를 수반합니다. | 핵의 분해와 관련이있다. |
에너지 | 낮은 에너지 변화. | 높은 에너지 변화. |
동위 원소 | 그들은 똑같이 반응한다. | 그들은 다르게 반응합니다. |
화학 조합 | 그것은 의존합니다. | 그것은 의존하지 않습니다. |
질량 | 반응물과 생성물의 질량은 동일합니다. | 대량 변경이 있습니다. |