주요한 차이점 : 이온 결합이란 하나의 원자가 다른 전자에 전자를 포기하는 두 개의 서로 다른 (즉, 금속과 비금속) 원자 사이의 화학 결합이다. 공유 결합은 또 다른 강한 화학 결합입니다. 그것은 유사한 원자 (즉 두 개의 비금속)가되었습니다. 공유 결합 (covalent bond)에서 두 원자는 서로 전자를 공유하는 원자 대신 전자를 공유하기 위해 모인다.
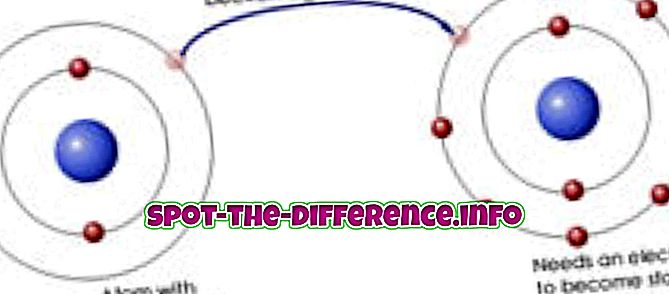
이온 결합이란 하나의 원자가 다른 전자에 전자를 포기하는 두 개의 서로 다른 (즉, 금속과 비금속) 원자 사이의 화학 결합이다. 따라서 두 원자는 하나의 원자가 하나의 전자를 가지고있을 때 이온이되고, 다른 하나는 여분을 갖는다. 전자를 잃은 금속 이온은 양전하를 띤다. 전자를 얻은 비금속 이온은 음전하를 띤다. 반대 이온들이 끌어 당길 때, 이 이온들은 강하게 서로 끌어 당겨 강하게 결합되어 결합하게됩니다.
이온 성 화합물은 일반적으로 고체, 즉 염의 형태로 존재합니다. 이들은 물에 잘 녹고 융점이 높습니다. 그들은 물에있을 때 높은 전기 전도도를 갖습니다.

공유 결합은 σ- 결합, π- 결합, 금속 - 금속 결합, 아고 스틱 상호 작용 및 3- 중심 2- 전자 결합을 포함하는 많은 종류의 상호 작용을 포함한다. 원자가 외부 껍질에 전자를 가지고 다른 원자가 외부 껍질을 채우기 위해 전자를 필요로 할 때, 두 원자는 함께 전자를 공유합니다. 따라서, 두 원자는 완전히 외부 껍질을 가지며 이에 상응하여 안정된 전자 배치를 갖는다.
화학 결합은 원자가 완전한 외부 껍질을 가질 수 있도록 만들어지며 완전한 외부 껍질은 안정된 전자 배치를 의미합니다. 이온 결합에서 금속 원자가 외부 껍질에 단일 전자를 가지고 비금속이 외부 껍질을 완성하기 위해 전자를 필요로 할 때 금속 원자는 전자를 비금속에 제공합니다. 마찬가지로, 공유 결합에서 그들은 전자를 똑같이 공유합니다.
이온 결합 | 공유 결합 | |
정의 | 서로 다른 두 원자 사이의 화학 결합으로 원자가 전자를 다른 전자로 포기합니다. | 공유 결합은 두 개의 유사한 원자 사이에서 전자를 공유하는 화학 결합이다. |
발생 | 금속 및 비금속 | 두 개의 비금속 |
극성 | 높은 | 낮은 |
분자의 형태 | 명확한 모양, 격자 구조 없음 | 명확한 모양 |
전기 전도도 | 높은 | 보통 없음 |
열 전도성 | 높은 | 일반적으로 낮음 |
물질의 융점 | 다양하지만 공유 결합 성 화합물보다 일반적으로 높다. | 다양하지만 보통 이온 성 화합물보다 낮음 |
물질의 끓는점 | 높은 | 다양하지만 보통 이온 성 화합물보다 낮음 |
물에서의 용해도 | 높은 | 다양하지만 보통 이온 성 화합물보다 낮음 |
상온에서의 물질 상태 | 보통 단색 | 고체, 액체, 기체 |